O tema da última aula,em geral, foi como distribuir os elétrons em subníveis de energia!
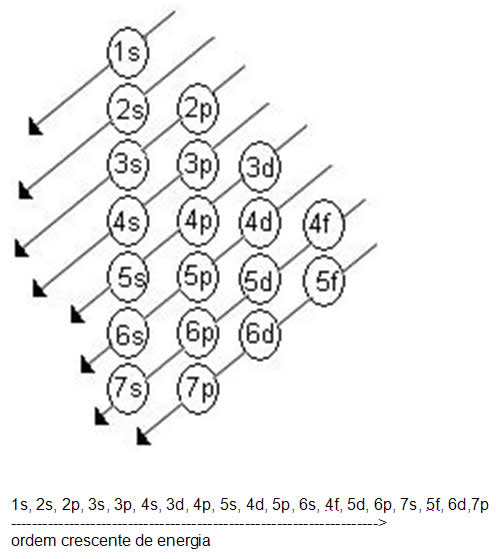
A forma com que fazemos isto é através do Diagrama de Pauling!
Não esqueçam de seguir as setas para realizar esta distruibuição!
Cada subnível comporta um determinado número de eletróns:
S: 2elétrons
P: 6 elétrons
D: 10 elétrons
F: 14 elétrons
Exemplo: Ca- Número Atômico =20
1s2
2s2 2p6
3s2 3p6
4s2
Não esqueçam também que nem sempre os elementos estão NEUTROS. Ou seja, nem sempre o número atômico, ou seja , o número de prótons, corresponde em igual ao número de elétrons!
Assim, quando eles não estiverem neutros...
Exemplo: Ca2+
No caso deste exemplo, o Cálcio está PERDENDO 2 elétrons.. (Na química, o símbolo de MAIS significa perder. E o símbolo de MENOS significa GANHAR).
Então, como ele está PERDENDO dois elétrons, nós devemos retirar os dois últimos elétrons da Camada de Valência
1s2
2s2 2p6
3s2 3p6
Então, o diagrama final do Ca2+ é:
1s2
2s2 2p6
3s2 3p6
E o contrário ocorrerá com elementos, a exemplo do Cl.
O Cloro tem número atômico igual a 17.
Então o diagrama seria:
1s2
2s2 2p6
3s2 3p5
Porém, na natureza, a tendência do Cloro é estar no estado Cl-.
Ou seja, ganhando um elétron!
Assim,no diagrama, devemos ADICIONAR um elétron a camada de valencia..
1s2
2s2 2p6
3s2 3p5 (+1)
Então, o resultado final é:
1s2
2s2 2p6
3s2 3p6
Precisamos lembrar também de dois conceitos que são muito utilizados quando falamos sobre Diagrama de Pauling.
Um dele é SUBNÍVEL MAIS ENERGÉTICO!
O subnível mais energético do Diagrama de Pauling é aquele em que se adicionou elétrons por último!
No Caso do Cl ,
1s2
2s2 2p6
3s2 3p5
O último subnível em que adicionamos elétrons é o 3p5, portanto este é o subnível mais energético!
No caso do Ca,
1s2
2s2 2p6
3s2 3p6
4s2
O subnível mais energético é o 4s2.
Outro conceito importante, é o conceito de CAMADA DE VALÊNCIA!
A camada de valência é a ultima camada em que aparece quando realizamos a distribuição eletrônica!
Observe os exemplos:
No caso do Cl
1s2
2s2 2p6
3s2 3p5
A camada de valência será 3s2 3p5.
No caso do Ca
1s2
2s2 2p6
3s2 3p6
4s2
A camada de valência será o 4s2 !
Bom, alunos, a matéria foi esta!
Estudem, realizem os exercícios complementares, e qualquer dúvida, me perguntem ou postem aqui.. Ou até mesmo me enviem um email em ana.barboza@usp.br.
Obrigada!
Prof. Ana
pra nao deixar a ana linda forever aqui (:
ResponderExcluireu estudei ta my love k
s2
Excluir